Al intervenir en la Mesa Redonda, la Dra. C. Miladys Limonta Fernández, coordinadora de Proyectos de Desarrollo de Candidatos Vacunales en el Centro de Ingeniería Genética y Biotecnología (CIGB), explicó cómo ocurre el desarrollo de un candidato vacunal desde las etapas tempranas.
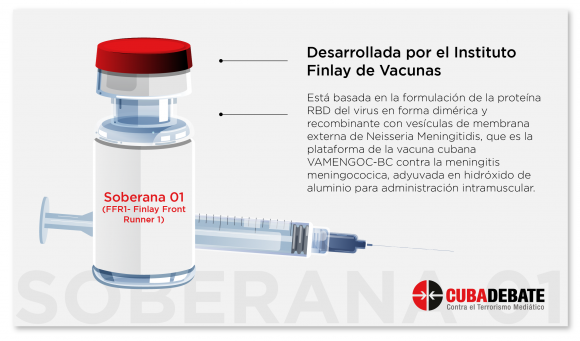
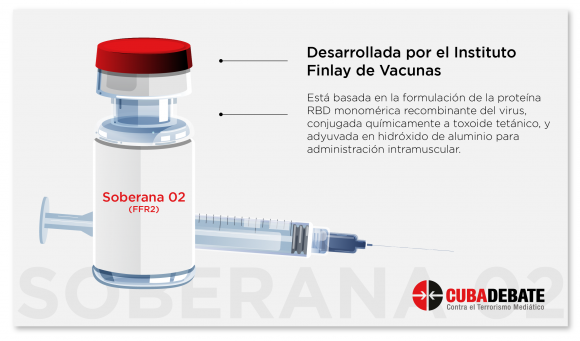
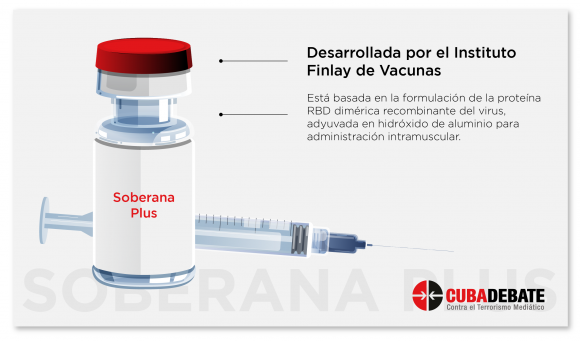
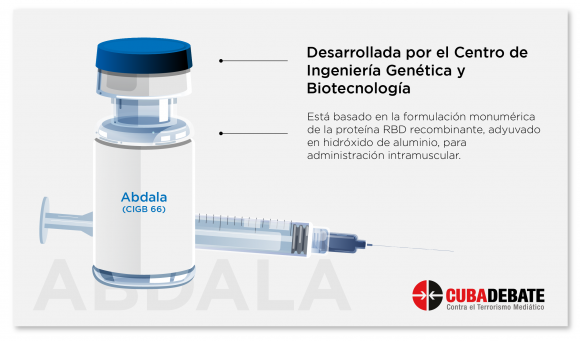
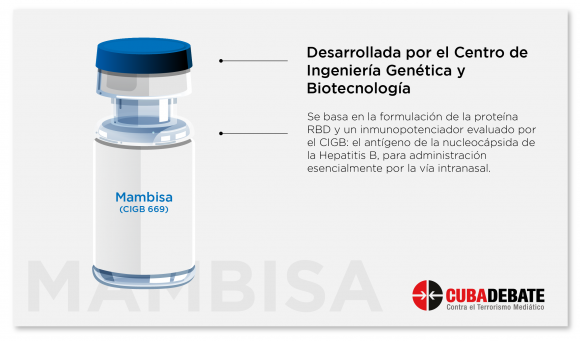
Tanto los candidatos vacunales Soberana como los del CIGB (Abdala y Mambisa) están basados en la proteína RBD, una parte del virus SARS-CoV-2. Esta estrategia estuvo basada en la plataforma de proteína de subunidad, y en fecha tan temprana como marzo de 2020, ya los biólogos moleculares del CIGB, y desde el diseño de computación, fueron trabajando en posibles proyectos.
“Al inicio teníamos 46 tipos de variantes, teniendo en cuenta las plataformas con que cuenta el CIGB. El centro cuenta con plataformas de expresión de proteínas en bacterias, en levaduras, en células de mamíferos (si bien no a la escala del CIM, en este caso específico), en plantas como biorreactores y en síntesis química.
Todas estas plataformas nos servían como una base para experimentar en cada una de las 46 variantes que estábamos trabajando al mismo tiempo”, dijo.
“En paralelo, teníamos también antecedentes en la historia del CIGB. El centro tiene entre sus plataformas de productos la vacuna contra la hepatitis B; además, la vacuna pentavalente, en la que se combinan cinco antígenos para combatir igual número de enfermedades; la vacuna del Haemophilus influenzae (que se trabajó en conjunto con la Universidad de La Habana y con el laboratorio de síntesis química de la UH, encabezado entonces por el doctor Vicente, hoy director del Instituto Finlay. También se incluyen el Heberbiovac HB y la HeberNasvac, que se utiliza para el tratamiento de la hepatitis B.
“Todos estos productos son parte de la plataforma del CIGB y, por tanto, constituían tecnologías que nosotros podíamos aprovechar para el desarrollo de cada uno de los candidatos vacunales de los que, en un futuro, íbamos a poder disponer para la población cubana”.
Otros de los productos de ese centro científico son el Nasalferón y Jusvinza, que han sido empleados en el combate contra la COVID-19 en Cuba. En el caso de Jusvinza, tiene plataforma en péptidos, mientras que el Herberferón y el Nasalferón tienen plataformas en bacterias.
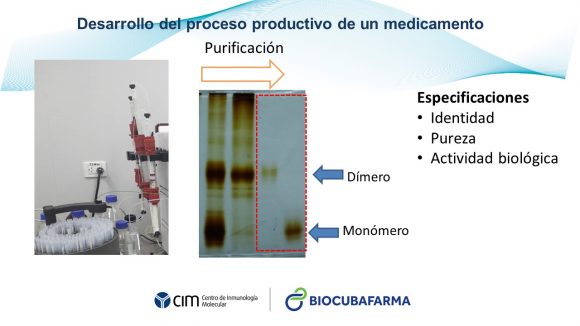
“El CIGB contaba con una historia muy amplia para abordar toda esta estrategia, teniendo en cuenta la estrategia de desarrollo tecnológico de un producto biofarmacéutico, que se divide en diferentes etapas: la analítica, la escala de banco y en la productiva, donde se producen cantidades diferentes de esos productos. En la escala analítica, son cantidades ínfimas.
“El proceso en esa escala (analítica) puede demorar dos o tres años, porque ahí se realiza el diseño de los experimentos. Es decir, ¿qué condiciones se le van a dar a la célula para que sea capaz de expresar esa proteína que se quiere que se produzca en ese microorganismo? Es ahí que intervienen diferentes variables: la temperatura, el oxígeno disuelto, el pH… En resumen, las condiciones ideales. Eso es lo que se trata de hacer en la escala del diseño experimental de cada una de las variables, donde se obtienen cantidades en microgramos.
Posteriormente transcurre la escala de banco, “donde se establecen las especificaciones. No se puede esperar a etapas tardías (en la escala productiva, por ejemplo) para establecer las especificaciones correspondientes. Debe hacerse en la etapa de banco.
“Pero, ¿qué sucedía? La RBD es una proteína de un virus totalmente nuevo. Entonces, había que trabajar en esta etapa en el establecimiento de las técnicas analíticas. Eso se hizo en paralelo.
“En esa misma etapa de banco es donde obtenemos el producto para hacer los estudios en animales, porque previamente al estudio clínico se requieren determinadas pruebas (toxicidad, seguridad del producto) que se realizan en animales, y en más de una especie. En esta etapa de banco, las cantidades están expresadas en miligramos y se estudia, asimismo, la estabilidad del producto, es decir, del ingrediente farmacéutico activo y después lo que viene a ser el producto.
“Es un proceso que toma tiempo, antes de llegar a la escala productiva, donde se obtiene el producto para el estudio clínico fase III, que es más amplio, y posteriormente se realizan el registro y la comercialización del producto terminado. En esta etapa las cantidades son de gramos. Incluso, hay condiciones productivas con las que se pueden obtener kilogramos de proteínas”.
En el desarrollo de los candidatos vacunales del CIGB, el cultivo se hizo en células de levaduras, con las cuales el centro tiene una gran experiencia de más de 30 años. Gracias a ello en 1991 se obtuvo la vacuna contra la hepatitis B, altamente reconocida a nivel mundial, cuya calidad es reconocida por un competidor, SmithKline, y que hoy es administrada a todos los niños al nacer.
Es un proceso que, además del escalado, incluye técnicas analíticas para medición de pureza, homogeneidad; la fortaleza para medir concentración y las dosis, además de técnicas para medir la seguridad (si el producto es estéril o no, si hay contaminantes como los pirógenos, causantes de fiebre.
“Algo nuevo, que necesitó de la acción coordinada y de la colaboración de varios centros, fue la obtención de materiales biológicos para el desarrollo de los ensayos específicos de los candidatos vacunales. Dependíamos de comprarlos en el exterior o producirlos nosotros mismos. Es la importancia de tener tantos centros científicos y un grupo como BioCubaFarma, esa visión de Fidel de contar con instituciones que pueden colaborar.
“El CIM se dispuso a desarrollar proteínas en células de mamíferos, que se utilizarían en el ensayo para determinar la cantidad de anticuerpos a evaluar ulteriormente por otras técnicas en el estudio clínico. De igual manera, en el CIGB de Sancti Spíritus se desarrollaron anticuerpos para las técnicas a utilizar en la determinación de contaminantes de hospederos. El Centro de Inmunoensayo está jugando igualmente un papel primordial, porque la capacidad de procesamiento que tiene ha permitido evaluar la cantidad de muestras en los estudios clínicos en curso y con una alta eficiencia.
“Igualmente, la colaboración del Centro de Investigaciones de la Defensa Civil permitió que, a partir del aislamiento del virus, se pudiera disponer de una técnica para hacer los estudios de capacidad de neutralización que tienen estos candidatos vacunales ante el reto del virus.
“Todas estas técnicas constituyeron una herramienta que posibilitó efectuar la caracterización físicoquímica del RBD que teníamos al día de hoy. Se va purificando toda la RBD hasta llegar a la pureza que tenemos hoy en el ingrediente farmacéutico activo (IFA) en el candidato vacunal, de más de 99% de pureza medida por diferentes técnicas.
“Después de que se tiene en la escala de banco un IFA en escalas de miligramos, es preciso proceder a los estudios no clínicos. A partir de que se van obteniendo las primeras cantidades, se empiezan a hacer los estudios de farmacología, de manera tal que permitan probar el concepto de la proteína que se está obteniendo. Es decir: ¿realmente levanta anticuerpos? Esa es una pregunta que debemos hacernos con este tipo de antígenos.
“Es una vacuna y las vacunas están diseñadas para levantar anticuerpos. Es importante medir entonces, en etapas tan tempranas, en especies de animales, este concepto.
“Igualmente es importante medir la toxicidad. ¿Cómo la medimos: con una dosis única, con dosis repetidas...? Es, precisamente, a partir de un diseño de dosis, hasta cien veces de las que vamos a usar en humanos, poderlas aplicar a un animal y ver el resultado. Eso se va haciendo desde esta etapa más temprana. Estudios de toxicidad a dosis repetidas, en primates no humanos, así como estudios de tolerancia local y de toxicidad de la reproducción en ratas. Son estudios no clínicos que se hacen a la par, previamente a la presentación del expediente”, explicó.
“Una vez que teníamos la proteína, hicimos la solicitud de aprobación de inicio de estudios clínicos ante la autoridad reguladora. En octubre del 2020,transferimos la producción de la escala de banco a la escala productiva en la planta del CIGB. Completada la escala productiva, se comienza, a partir de la aprobación de la autoridad reguladora, los estudios clínicos de Abdala”.
Sobre la evolución clínica de este candidato vacunal, señaló que el 7 de diciembre comenzaron los ensayos clínicos de Abdala y Mambisa. Las fases I y II de Abdala transcurrieron entre diciembre y marzo. El 1ro. de mayo, en el fase III, debe administrarse la tercera dosis, tras comenzar su aplicación el 19 de abril.
“Marzo de 2021 −recordó− marcó el inicio del escalado final del IFA de Abdala, en el fermentador de 3 000 litros”.
La directiva destacó también el candidato vacunal Mambisa, el cual incluye también en su composición como ingrediente farmacéutico activo el RBD, y que es uno de los cinco candidatos vacunales en el mundo que utilizan la vía nasal. “Terminamos el ensayo clínico fase I en el que se demostró en 88 individuos su seguridad y tolerancia”.
Actualmente, transcurre el proceso para presentar ante la autoridad reguladora un estudio, fases I-II, para emplear ese candidato vacunal como dosis de refuerzo en convalecientes. La vía de administración es nasal.
“Otra aplicación de Mambisa puede ser como dosis de refuerzo en la combinación de otras vacunas. Por ejemplo, Sputnik V, la vacuna rusa, pudiera combinarse con Mambisa, y quizás en un futuro transnacionales como Pfizer y Moderna podrían interesarse.
“Cuba es el único país del mundo que se ha ocupado de los convalecientes y de este tipo de aplicación”, subrayó.
Estudios han demostrado cómo las dosis de refuerzo elevan los niveles de anticuerpos en las personas. “Esto va en sintonía con lo que estamos aplicando, al utilizar dosis de refuerzo en esquemas de vacunación desde el principio”.
Por último, informó que el CIGB está trabajando en relación con las variantes. “Es decir, a esta misma proteína se le incluye la información genética de los mutantes (B1-7 y B1-351). A partir de abril se va a trabajar en el escalado de ese posible candidato que incluye los mutantes, porque la plataforma tecnológica nos permite avanzar en esta dirección con las tecnologías que dominamos”.
CUBADEBATE





1- Que no debe utilizar un lenguaje ofensivo.
2- Que debe ajustarse al tema del artículo.
El administrador del portal se reserva el derecho a no publicar los comentarios que incumplan las políticas anteriores.